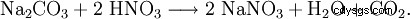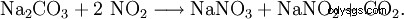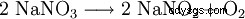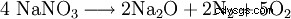| 構造式 | |||||||
|---|---|---|---|---|---|---|---|
| そうですね | |||||||
| 全般 | |||||||
| 名前 | 硝酸ナトリウム | ||||||
| 他の名前 |
| ||||||
| 分子式 | NaNO3 | ||||||
| CAS 番号 | 7631-99-4 | ||||||
| 簡単な説明 | 無色の結晶性固体 | ||||||
| プロパティ | |||||||
| モル質量 | 84.99 g mol | ||||||
| 物質の状態 | 修正済み | ||||||
| 密度 | 2.26 g cm | ||||||
| 融点 | 306.8 °C | ||||||
| 沸点 | 380 °C からの分解 | ||||||
| 蒸気圧 | <0.001hPa (25°C) | ||||||
| 溶解度 | 水に溶けやすい:874 g/l (20 °C) | ||||||
| 安全上の注意 | |||||||
| |||||||
| MAK | 指定なし | ||||||
| LD50 | 1267 mg kg (ラット、経口) | ||||||
| 可能かつ一般的な場合、SI 単位が使用されます。特に明記しない限り、与えられたデータは標準的な条件下で適用されます。 | |||||||
硝酸ナトリウム (また硝酸ナトロン またはチリの硝石 ) は化学化合物、硝酸のナトリウム塩です。純粋な状態では、吸湿性 (吸水性) の白い物質または無色の結晶の形をしています。
オカレンス
硝酸ナトリウムは、天然に存在する最も重要な硝酸塩です。主な産地はチリであるため、一般名はチリ硝石です。他にもエジプト、小アジア、コロンビア、カリフォルニアに天然鉱床があります。
抽出
自然堆積物は、熱水で浸出することによって得られた熱塩水を濾過することによって、異物を取り除きます。低温で結晶化する硝酸ナトリウムの純度は約98%です。母液に含まれるヨウ素酸塩は、ヨウ素抽出に使用されます。
硝酸ナトリウムは、炭酸ナトリウムと硝酸を反応させることでも得られます。
ここでは、濃縮炭酸ナトリウム溶液でのアンモニアの酸化による残留ガスの吸収が理想的です。
亜硝酸塩を酸化するには、硝酸で酸性化し、空気中で硝酸塩に酸化し、炭酸ナトリウムで中和します。真空蒸発器で濃縮して固体にします。
プロパティ
物性
- 重要な熱力学的特性
- Δf Hさん :15.5 in kJ/mol
- Ss :116 in J/(mol K)
化学的性質
熱硫酸では、硝酸を形成して硫酸水素ナトリウムに変換されます。
380 °C を超える温度では、亜硝酸ナトリウムに分解します:
800 °C を超える温度で酸化ナトリウムに:
使い方
- 肥料
- 建材産業:セメント添加剤
- 化学製造:硝酸カリウム
- 以前は硝酸の製造にも使用されていました
- 防腐剤E 251として
- 肉およびソーセージ製品の硬化用 (亜硝酸ナトリウム E 250 および亜硝酸カリウム E 249 も含む)
- 蓄熱用PCM
食品添加物
硝酸塩はバクテリア、特に恐ろしいボツリヌス菌(ボツリヌス菌)に対して作用します。硬化プロセス中に、化学的に安定性の低い筋肉色素 (ミオグロビン) が、より安定した変種 (赤化) に変換されます。その結果、肉は赤い色を保ちます。硬化していない肉やソーセージは、ほとんどの消費者が腐敗の兆候と誤解する灰色に変わります.さらに、硬化中に典型的な香りが形成されます。
硝酸ナトリウムは、ソーセージ、ハード チーズ、セミハード チーズ、ニシンのピクルス、スプラットに使用されます。
硝酸塩自体は無害です。それらは亜硝酸塩に変換されるため、それらの使用には問題があります。この変換は食品だけでなく、人体でも可能です. 亜硝酸塩には血管拡張作用と血圧降下作用があります.高用量では、中毒の急性症状を引き起こす可能性があります。 (血液色素ヘモグロビンの欠乏=青中毒)。亜硝酸塩は、タンパク質の吸収と同時に人体で発がん性の高いニトロソアミンに変換される可能性があります.
証明
- 検出反応
- ナトリウム:青いブンゼン バーナーの炎の中の明るい黄色のように
- 硝酸塩:物質のヘラの先端を希硫酸に溶かし、冷たい飽和硫酸鉄(II)溶液を加えます。少量の濃硫酸で下塗り。茶色のリングが境界層に形成されます。これは硝酸塩の証拠です (リング テスト)。