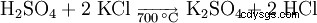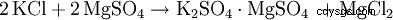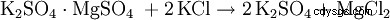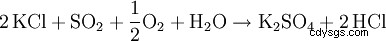| 構造式 | |
|---|---|
| 全般 | |
| 名前 | 硫酸カリウム |
| 他の名前 |
|
| 分子式 | K |
| CAS 番号 | 7778-80-5 |
| 簡単な説明 | 無色の結晶または粉末 |
| プロパティ | |
| モル質量 | 174.26 g/モル |
| 物質の状態 | 修正済み |
| 密度 | 2662 kg/m³ |
| 融点 | 1069 °C |
| 沸点 | 1689 °C |
| 蒸気圧 | - |
| 溶解度 | 111.1 g/l (20 °C の水) 250 g/l (100 °C の水)、エタノールに不溶 |
| 安全上の注意 | |
| 危険のシンボル | |
| - | |
| R および S フレーズ |
R:リスク フレーズなし |
| MAK | - |
| 可能かつ一般的な場合は、SI 単位が使用されます。特に明記しない限り、与えられたデータは標準的な条件下で適用されます. | |
硫酸カリウム 、分子式 K
歴史
薬剤師であり化学者でもある Johann Rudolph Glauber は、14 世紀から知られていた塩化カリウムと硫酸から塩を最初に製造した.
オカレンス
硫酸カリウムは、いわゆる複塩の形でさまざまなミネラルに含まれています。この例は、シェーナイト、レオナイト、ラングベイナイト、ポリハライト、グラセライトです。
外観
当初、硫酸カリウムは鉱物カイナイト (MgSO4 ・KCl ・3H2 O) 勝ちました。しかし、この製造方法はすぐに放棄され、塩化カリウムに基づくより費用対効果の高いプロセスが採用されました.
硫酸カリウムの生成における 1 つの可能性は、700 °C の温度での塩化カリウムと硫酸との反応です。
あるいは、硫酸カリウムは、他の金属硫酸塩などと二重反応する。 B. 硫酸マグネシウム:
いわゆるハーグリーブス法では、塩化カリウムと二酸化硫黄、空気、水の混合物を反応させて硫酸カリウムを生成します。
硫酸カリウムは、硝酸生産の副産物でもあります。
硫酸カリウムは、水酸化カリウムと硫酸を反応させることで生成しやすくなります。
プロパティ
無水結晶は、本質的に菱形です。それらは無色透明で、非常に硬く、空気中で非常に安定しています。硫酸カリウムの味は苦味から塩味です。水に溶けますが、エタノールには溶けません。
使い方
硫酸カリウムは、カリミョウバン、カリ水ガラス、過硫酸カリウム、カリ、フレグメーター、ミネラルウォーター、合成ゴム、および混合肥料の製造に使用されます。また、酒石酸および酒石酸の精製や、染料、爆発物、製薬業界でのさまざまな用途にも使用されています。
硫酸カリウムは、ダイエット食品の食塩の代用として使用されています。また、塩化物に敏感な植物培養物を肥やすために使用されるカリ肥料の成分でもあります。 B. ブドウ栽培に使用する
EU では食品添加物として番号 E 515 を持っています 承認されました。
硫酸カリウムは、クラス B および C 消火粉末の有効成分としても使用されています。
ソース
<オール>Holleman、Wiberg、無機化学の教科書 、deGruyter Verlag、第 101 版、p. 1179