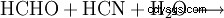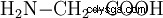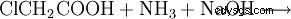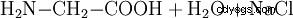| 構造式 | ||
|---|---|---|
| 全般 | ||
| 名前 | グリシン | |
| 略語 | Gly、G | |
| レストネーム | グリシル | |
| 必須 | いいえ | |
| 他の名前 | グリコール、グリコール、アミノ酢酸 | |
| 分子式 | C2 H5 NO2 | |
| CAS 番号 | 56-40-6 | |
| 簡単な説明 | 白い固体 | |
| プロパティ | ||
| モル質量 | 75.07 g/mol | |
| 物質の状態 | 修正済み | |
| 密度 | 1.595g/cm | |
| 融点 | 450-500°F | |
| 沸点 | > 230 °C 熱分解 | |
| 蒸気圧 | Pa (°C) | |
| 側鎖 | 側鎖なし、それ以外は親水性 | |
| 溶解度 | 水によく溶ける (20 °C で 225 g/l)、 アルコールに溶けにくく、非極性溶媒に不溶 | |
| 等電点 | 6.06 | |
| pK 値 25 °C で | pK | |
| ファン デル ワールスの巻 | 48 | |
| 疎水性評価 | −0.4 | |
| 安全上の注意 | ||
| ||
| R および S フレーズ | R:リスク フレーズなし S:S フレーズなし | |
| MAK | 未設定 | |
| 可能かつ一般的な場合は、SI 単位が使用されます。特に明記しない限り、与えられたデータは標準的な条件下で適用されます。 | ||
グリシン (化学的にアミノ酢酸と呼ばれる) は、最小かつ最も単純なタンパク質構成アミノ酸です。これは親水性アミノ酸のグループに属し、キラルではなく、したがって光学活性でない唯一のタンパク質構成アミノ酸です。
グリシンは必須ではないため、人体自体によって生成される可能性があり、ほぼすべてのタンパク質の重要な構成要素であり、代謝における重要なノードです.
名前は、純粋なグリシン (gr. glycis) の甘い味に由来します。 : 甘い)。
合成
グリシンは、とりわけ、ホルムアルデヒド、シアン化水素、および水の反応で形成されます。
この反応は、約 40 億年前に地球を取り囲んでいたいわゆる原始大気から出発物質が形成された可能性があるという仮説により、特に重要です。彼女はおそらく水素 (H2 )、ヘリウム (He)、および少量のメタン (CH4 )、アンモニア (NH3 ) とその他の希ガス。
化学的に、グリシンはモノクロロ酢酸とアンモニアからも調製できます。
体内では、ほとんどのグリシンは食物から得られますが、セリンからも作ることができます.
関数
代謝
グリシンの生成に加えて、セリンからグリシンへの変換は、テトラヒドロ葉酸を N-N-メチレン-テトラヒドロ葉酸に変換する役割も果たします。これは、とりわけ、チミン ヌクレオチド (DNA 成分) の合成に必要です。
グリシンは、遺伝物質の他の成分 (プリン) の合成にも直接必要です。また、ヘム (血液中の酸素結合)、クレアチン (筋肉内のエネルギー貯蔵)、またはグルタチオンの生合成にも役立ちます。
いわゆる糖原性アミノ酸として、グリシンは代謝の一部としてピルビン酸を介してグルコースに変換されます。
有毒なシュウ酸は、副産物としてグリシンから形成されることもあります.
これは、動物生物で最も一般的なタンパク質であるコラーゲンで特に一般的です.ここでは、全アミノ酸の 3 分の 1 を占めています。これは、サイズが小さいため、コラーゲンが三重らせん構造に巻き込まれるためです.
神経系
グリシンは、グリシン受容体を介して中枢神経系で抑制性神経伝達物質、すなわち抑制性シグナル伝達物質として作用します。リガンド依存性クロライド チャネルを開くことによって作用し、抑制性シナプス後電位 (IPSP) を引き起こし、下流のニューロン活動を低下させます。
グリシン放出神経細胞 (グリシン作動性ニューロン) は、主に脊髄に見られ、前角のいわゆる運動ニューロンを阻害し、細胞によって神経支配される筋肉の筋肉活動を低下させます。
グリシン受容体のアンタゴニストであるストリキニーネと、グリシンの放出を阻害する破傷風毒素は、グリシンの効果を低下させます。抑制が失われると、筋肉の活動が増加します。これは生命を脅かすけいれんにつながる可能性があります.
使い方
グリシンは風味増強剤として食品に添加されます。
グリシンとそのナトリウム塩は、EU で食品添加物として E 640 に指定されています 通常、最大量制限のない食品として承認されていますが、健康への影響は不明です。
参考文献
- G. Löffler、P. E. Petrides:生化学および病態生化学 、第 7 版、Springer Verlag、2003 年、ISBN 3-540-42295-1