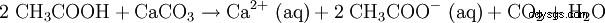| 構造式 | |||||||
|---|---|---|---|---|---|---|---|
| 全般 | |||||||
| 名前 | 酢酸 | ||||||
| 他の名前 |
| ||||||
| 分子式 | C2 H4 O2 | ||||||
| CAS 番号 | 64-19-7 | ||||||
| 簡単な説明 | 刺激臭のある無色の液体 | ||||||
| プロパティ | |||||||
| モル質量 | 60.05 g mol | ||||||
| 物質の状態 | 液体 | ||||||
| 密度 | 1.05g cm | ||||||
| 融点 | 17℃ | ||||||
| 沸点 | 118℃ | ||||||
| 蒸気圧 | 16hPa (20°C) | ||||||
| pKa値 | 4.75 | ||||||
| 溶解度 | 水と完全に混和します (20 °C) | ||||||
| 安全上の注意 | |||||||
| |||||||
| MAK | 未設定 | ||||||
| 熱力学的特性 | |||||||
| ΔHf | −483.52 kJ mol | ||||||
| 可能かつ一般的な場合、SI 単位が使用されます。特に明記しない限り、与えられたデータは標準的な条件下で適用されます。 | |||||||
酢酸 、IUPAC 規制による エタン酸 は無色の液体の苛性カルボン酸で、典型的な酢の匂いがします。食品添加物として、それは指定E260を持っています.酢酸の水溶液は、自明に酢と濃酢酸氷酢酸と呼ばれるだけです.酢酸のラテン名は Acidum acetum です。 .酢酸塩は酢酸塩と呼ばれます 専用。生化学では、酢酸という用語は酢酸の用語よりも好まれます。これは、酢酸が酢酸アニオン (CH
取得と表示
伝統的なオーガニック生産
酢酸の古典的な生産は発酵です。アセトバクター細菌は、他の発酵プロセスで生成されたエタノール (アルコール) を酢酸 (発酵酢) に変換します。製品を開始することができます。 g. ワイン、ビール、麦芽家庭用酢 発酵酢または希釈合成酢で構成され、5%の酢酸が含まれています。 酢のエッセンス 25% の合成酢酸水溶液で、強い刺激臭があり、食品に希釈してのみ使用できます。
大規模な化学製造
酢酸の最も重要な工業的合成は、加圧下での一酸化炭素によるメタノールの触媒変換です (モンサント法)。
CH3OH + CO → CH3COOH
これとは別に、Mn(OAc)2を用いてアセトアルデヒドを空気または酸素で酸化して酢酸を合成することもできる。 触媒として、または他の炭化水素の部分酸化によって。
技術的には、約 180 °C および 85 バールでの n-ブタンの空気酸化と軽質ガソリンの触媒酸化も使用されます。
プロパティ
物理的特性
酢酸が水に溶けると、約100分の1の酢酸分子が解離して酢酸イオンを形成します。分裂したプロトンは水分子に移動します。このプロセスで形成されるオキソニウム イオンは、酢酸溶液の酸性特性を引き起こします。
酢酸は 118 °C で、同等のモル質量を持つ極性物質と比較して比較的高い沸点を持っています (例:1-プロパノール:沸点 97 °C)。この理由は、酢酸分子がそのカルボキシル基を介して 2 つの「相互」水素結合を形成できるため、2 つの酢酸分子から二量体が形成され、モル質量の 2 倍の分子のように振る舞います。したがって、これらの二量体を気相に移動させるには、より高い量のエネルギーが必要であり、これは沸点の「上昇」によって認識できます。
化学的性質
酢酸は空気中で完全に酸化して、水と二酸化炭素を生成します。
マグネシウム、カルシウム、亜鉛、鉄などの卑金属は、希酢酸に溶解して水溶性の酢酸塩を形成し、水素を放出します。
酢酸は、酸素 (空気) の存在下で銅と反応して、緑青としてよく知られている緑色の有害な塩である酢酸銅を形成します。
酢酸はエタノールと反応して、広く使用されている溶媒である酢酸エチルを形成します。 1-ペンタノールをエタノールに置き換えると、強いにおいのエステルである酢酸アミルが得られます。サリチル酸は酢酸でエステル化することもできます。これにより、アスピリンの有効成分であるアセチルサリチル酸が生成されます。
酢酸は 800 °C で無水酢酸に脱水反応します。
希酢酸は、石灰スケールを溶解するためにも使用されます (酢を参照)。反応方程式は次のようになります:
熱力学的特性
1 bar における液体の標準エントロピー (Sl, 1 bar ) は 158.0 J mol K であり、固体 (Ss ) 282.84 J mol K.
使い方
酢酸は香料として非常に重要です。酢酸およびその塩である酢酸カリウム (E 261)、酢酸ナトリウム (E 262)、および酢酸カルシウム (E 263) は、あらゆる種類の缶や瓶に入った果物や野菜の酸味料として使用されます (0.5–3% 酢酸)。魚、ジャム、さまざまなマリネ、デリカテッセン サラダ、マヨネーズ、ソルビン酸 (E 200) または安息香酸 (E 210) と一緒のサラダ ドレッシング、新鮮な肉のピクルスと洗浄用。
酢酸の殺菌効果は、変化した pH 値が生理学的プロセスを防ぎ、タンパク質を変性させることです。
酢酸は化粧品 (クリーム、石鹸) の製造にも使用されます。
酢酸塩 (酢酸塩)
酢酸の塩またはエステルはアセテートと呼ばれます 専用。それらは酢酸陰イオン (CH3 COO).
塩状酢酸塩の例は、酢酸ナトリウム (NaCH
塩状の酢酸塩は、酢酸を金属水酸化物または金属酸化物で中和することによって得られます。
-
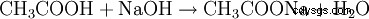
- 酢酸と水酸化ナトリウムが反応して、酢酸ナトリウムと水が形成されます。
-
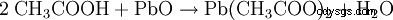
- 酢酸と酸化鉛(II)は、酢酸鉛と水を生成します。
化学分析では、サンプルを乳鉢で硫酸水素カリウムと一緒に粉砕することにより、酢酸塩を簡単に検出できます。このプロセスでは、硫酸水素イオンのプロトン (H) が酢酸イオンに移動し、揮発性の酢酸が生成されます。これは、その特徴的な臭いによって簡単に識別できます。
-

- アセテートは硫酸水素塩によってプロトン化されます。酢酸と硫酸塩が形成されます。
酢酸エステルは、酸基としてアセチル基を含む。これらのエステルの中で最もよく知られているのは酢酸エチルです。有機アセテートは、酢酸をアルコール (R-OH) でエステル化することによって得られます。
-

- 酢酸とアルコールは反応して酢酸エステルと水を形成します。