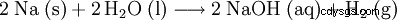| 構造式 | |||||||
|---|---|---|---|---|---|---|---|
| 全般 | |||||||
| 名前 | 水酸化ナトリウム | ||||||
| 他の名前 | 苛性ソーダ、苛性ソーダ、苛性ソーダ、石鹸石、水酸化ナトリウム、水酸化ナトリウム、苛性ソーダ(水溶液)、E 524 | ||||||
| 分子式 | NaOH | ||||||
| CAS 番号 | 1310-73-2 | ||||||
| 簡単な説明 | 白色の結晶性固体、しばしばペレットの形をしている | ||||||
| プロパティ | |||||||
| モル質量 | 39.997 g mol | ||||||
| 物質の状態 | 修正済み | ||||||
| 密度 | 2,130 g cm | ||||||
| 融点 | 322°C | ||||||
| 沸点 | 1388℃ | ||||||
| 蒸気圧 | 13 Pa (618 °C) | ||||||
| 溶解度 |
水に易溶: | ||||||
| 安全上の注意 | |||||||
| |||||||
| MAK | 指定なし | ||||||
| WGK | 1 – 水にわずかに危険 | ||||||
| 可能かつ一般的な場合、SI 単位が使用されます。特に明記しない限り、与えられたデータは標準的な条件下で適用されます。 | |||||||
水酸化ナトリウム (また苛性ソーダ 、苛性ソーダ )、化学式 NaOH
2001 年の世界の生産量は 4,600 万トンでした。
製造
- 炭酸ナトリウムと水酸化カルシウムの反応による水酸化ナトリウムと炭酸カルシウムの生成:
わずかに溶解する炭酸カルシウムを濾別する。容易に溶解する水酸化ナトリウムはろ液に残ります。
- 塩化ナトリウムから苛性ソーダ、水素、塩素ガスへの電気分解 (塩素アルカリ電気分解)
いくつかの産業プロセスがあります:
<オール>(クロルアルカリ電解も参照)
すべてのプロセスに共通するのは、無水水酸化ナトリウムに到達するための追加の精製および濃縮ステップです。
- 水酸化ナトリウムは、実験室でナトリウム元素を水と反応させて苛性ソーダと水素を生成することによって得ることができます。
- 苛性ソーダが蒸発した後、固体の水酸化ナトリウムが残ります:
使い方
- 各種石鹸(苛性ソーダ)の製造
- 染料(苛性ソーダ)の製造
- 木材とわらからのセルロースの生産
- 綿のマーセライズ
- グリース、オイル、石油の洗浄
- ボーキサイトの消化 (アルミニウム生産の前駆体)
- さまざまな化学物質の合成 (例:次亜塩素酸ナトリウム、リン酸ナトリウム、硫化ナトリウム、アルミン酸ナトリウム)
- ギ酸の合成
- 脱イオン水の生成:イオン交換体の再生
- 電子機器における露出したプリント基板材料の開発 (20°C で約 10g/l)
- 排水管クリーナーの一部
- 茶色の色と「ソープ」味のプレッツェルを作る
- 実験室および水族館のニーズに合わせた脱イオン装置の再生
- 模型メーカー向けの真鍮、洋白、銅板のエッチング
- ブルーライを使用したワインの酸度の測定
- ステンレスタンクの洗浄
- 古いペンキの除去 (ストリッピング)
- 縮毛矯正用(リラクサー)
- ナトロン機関車
- すべての有機窒素化合物の検出 (「マヌート検出」)
- 産業処理中の果物や野菜の皮の除去 (!)
- 鋼を硬化させるために水に溶かしたクエンチャント
実験例
水に少量の水酸化ナトリウムを加えてかき混ぜると、溶液が温まります。これは、たとえば学校で使用される発熱ソリューション プロセスの簡単な例として適しています。硝酸カリウムまたは硝酸アンモニウムを水に溶解すると、反対の効果である吸熱溶解プロセスが観察され、硝酸アンモニウムを溶解すると、その効果ははるかに強くなります (約 10 K の温度低下)。
ソース
<オール>- ナトリウム